Общие свойства растворов. Типы растворов, термодинамика растворения
Общие свойства растворов.
Растворы – это однофазные (гомогенные) системы, состоящие из двух и более компонентов (составных частей) и продуктов их взаимодействия.
В природе и в промышленности растворы имеют огромное значение. Растения усваивают питательные вещества в виде растворов. Усвоение пищи связано с переводом этих веществ в раствор. Все природные воды являются растворами. Важнейшие физиологические жидкости - кровь, лимфа и др. –
также растворы. Большинство химических реакций протекает в растворах.
Растворы могут существовать в любом из агрегатных состояний: газообразном, жидком или твердом. Например, морская вода - это водный раствор различных солей. Металлические сплавы - твердые растворы одних металлов в других. Итак, любой раствор состоит, как минимум, из двух индивидуальных веществ, одно из которых считают растворителем, а другое - растворенным веществом. Между тем, такое деление очень условно, а для веществ, смешивающихся в любых соотношениях (вода - ацетон, золото - серебро) лишено смысла.
Способность к образованию растворов выражена в различной степени у различных индивидуальных веществ. Одни вещества способны растворяться друг в друге неограниченно (вода и спирт), другие - лишь в ограниченных количествах (поваренная соль в воде).
Раствор, в котором данное вещество при данной температуре уже больше не растворяется, т.е. раствор, находящийся в равновесии с растворяемым веществом, называют насыщенным.
В насыщенном растворе при данной температуре содержится максимально возможное количество растворенного вещества.
Если раствор, насыщенный при нагревании, осторожно охладить до комнатной температуры (так, чтобы не выделялись кристаллы соли), то образуется пересыщенный раствор. Таким образом, пересыщенным называют раствор, в котором при данной температуре содержится большее количество растворенного вещества, чем в насыщенном растворе. Пересыщенный раствор нестабилен, и при изменении условий (например, энергичное встряхивание или внесение кристаллика соли - затравки для кристаллизации) образуется насыщенный раствор и кристаллы соли, содержащейся в избытке. Пересыщенные растворы образуют сахароза, и др.
Малорастворимые и практически нерастворимые вещества часто
объединяют одним названием - малорастворимые. Тогда говорят только о
растворимых и малорастворимых веществах.
Растворимость
Количественно растворимость того или иного вещества выражается концентрацией насыщенного раствора. Чаще всего ее выражают при помощи массы вещества, которая может растворяться в 100 г воды при данной температуре, и иногда называют коэффициентом растворимости или просто растворимостью вещества. Так, например, при 18° С в 100 г воды растворяется 51,7 г соли нитрата свинца (II) (т.е. растворимость этой соли при 18° С равна 51,7). Если при той же температуре сверх этой массы добавить еще соль нитрата свинца (II), то она не растворяется, а выпадает в виде осадка.
Говоря о растворимости вещества, следует указывать температуру при растворении. Чаще всего растворимость твердых веществ с увеличением температуры возрастает.
В отличие от большинства твердых тел растворимость газов в воде с повышением температуры уменьшается, что обусловлено непрочностью связи между молекулами растворенного газа и растворителя.
Другой важной закономерностью, описывающей растворимость газа в жидкостях, является закон Генри: растворимость газа прямо пропорциональна его давлению над жидкостью.
Эта закономерность выражается формулой:
x= kр,
где х - молярная доля растворенного вещества; р - давление; k - постоянная величина.
Следует отметить, что причины различной растворимости веществ до настоящего времени до конца не выяснены. Между тем, еще до обоснования теории растворов опытным путем было установлено правило, согласно которому подобное растворяется в подобном. Так, вещества с ионным типом связи (соли, щелочи) или полярным (спирты, альдегиды) хорошо растворимы в полярных растворителях, в первую очередь в воде. Например, метиловый, этиловый и пропиловый спирты смешиваются с водой в любых соотношениях. По мере дальнейшего увеличения углеводородного радикала в молекуле ROH происходит уменьшение полярности связи О-Н и растворимость спиртов в воде и воды в спиртах понижается. И наоборот, растворимость кислорода в бензоле на порядок выше, чем в воде, так как их молекулы ( и ) неполярны. Вместе с тем аммиак, молекулы которого полярны, намного лучше растворяется в воде, чем в неполярных органических растворителях.
Важной характеристикой любого раствора является его состав. Существуют различные способы численного выражения состава растворов: массовая доля растворенного вещества, молярная концентрация и др.
Массовая доля растворенного вещества - это безразмерная физическая величина, равная отношению массы растворенного вещества к общей массе раствора, т.е.
где - массовая доля растворенного вещества; - масса растворенного вещества m - общая масса раствора.
Массовую долю растворенного вещества обычно выражают в долях единицы или в процентах. Например, если массовая доля серной кислоты в воде равна 0,05, или 5%, это означает, что в растворе серной кислоты массой 100г содержится серная кислота массой 5г и вода массой 95г.
Для количественной характеристики растворов используется понятие концентрация - величина, характеризующая число частиц, отнесенное к единице объема. В химии концентрацию обычно измеряют не числом частиц, а числом молей в единице объема. Чаще всего используют молярную концентрацию.
Типы растворов. По количеству растворенного вещества растворы могут быть разбавленными (в одном литре разбавленного раствора содержится менее одного моля растворенного вещества) и концентрированными.
По количеству растворенного вещества и характеру установившегося равновесия между растворенным веществом и растворителем растворы делятся на ненасыщенные, насыщенные и пересыщенные (раздел 8.4).
По результату взаимодействия вещества с растворителем растворы делят на ионные (в них растворяемое вещество частично или полностью диссоциировано на ионы) и молекулярные (растворяемое вещество распределяется в растворителе в виде отдельных молекул).
По электрической проводимости растворы делятся на:
растворы неэлектролитов, не способные проводить электрический ток (молекулярные растворы);
растворы электролитов, проводящие электрический ток (ионные растворы, проводники второго рода).
Растворенные вещества делятся, в свою очередь, на неэлектролиты и электролиты.
Неэлектролиты – это вещества, которые в растворе и расплаве не диссоциируют (не распадаются) на ионы.
Электролиты – это вещества, которые в расплавах, воде и других полярных растворителях диссоциируют на ионы.
Общие свойства жидких растворов. Все растворы обладают рядом общих свойств:
1. Давление насыщенного пара растворителя над раствором всегда ниже, чем над чистым растворителем; при этом, чем больше концентрация растворенного вещества, тем давление ниже (это свойство описывает Iзакон Рауля).
Насыщенный пар – это пар, находящийся в равновесии с жидкостью; V исп =V конд.
2. Растворы всегда кипят при температурах более высоких, а замерзают при более низких, чем чистый растворитель (это свойство описывает IIзакон Рауля).
3. Для растворов характерно явление осмоса (это свойство описывает закон Вант-Гоффа).
Эти свойства количественно зависят от числа частиц растворенного вещества, от концентрации раствора и от того, является ли данный раствор раствором электролита или неэлектролита.
Для количественного описания свойств растворов используют модель идеального раствора. Если при образовании раствора тепловой эффект ∆Н=0, изменение объема ∆V=0, изменение энтропии ∆S= ∆Sидеального раствора, то раствор называют идеальным. В идеальном растворе между компонентами нет химического взаимодействия; каждый компонент ведет себя в идеальном растворе независимо от остальных компонентов, и свойства раствора при данных условиях определяются только концентрацией растворенного вещества. Из реальных растворов лишь разбавленные растворы неэлектролитов могут по своим свойствам приближаться к идеальным.
Примерами растворов неэлектролитов могут служить, например, растворы кислорода и сахара в воде, водные растворы органических спиртов, растворы углеводородов в углеводородах и т.д.
8.7. Свойства растворов неэлектролитов
Давление насыщенного пара над раствором. I закон Рауля.
В результате естественного процесса испарения над жидкостью образуется пар, давление которого можно измерить с помощью манометра (рис. 8.1). Эндотермический процесс испарения обратим; одновременно с ним протекает экзотермический процесс конденсации:

При равновесии (∆G=0) V исп =V конд. Каждый раствор находится в равновесии с его насыщенным паром. Давление насыщенного пара каждого вещества есть величина постоянная при данной температуре, с повышением температуры давление пара увеличивается.
Давление насыщенного пара жидкости определяется числом молекул жидкости, отрывающихся с ее поверхности за единицу времени.
Рассмотрим пример (рис.8.2). В первом сосуде у нас находится чистая вода, во втором – раствор сахара в воде (раствор неэлектролита; сахар -- нелетучее вещество и при данных условиях не испаряется).
При образовании раствора концентрация растворителя уменьшается, его мольная доля становится меньше единицы (N 1 <1). Поверхность раствора, в отличие от поверхности чистого растворителя, частично занята молекулами нелетучего растворенного вещества. Это приводит к уменьшению числа молекул растворителя, испаряющихся в единицу времени.

Однако основную роль здесь играют силы сольватационного взаимодействия между молекулами растворителя и растворенного вещества. Эти силы значительно прочнее сил сцепления между молекулами растворителя, чем и объясняется переход меньшего числа молекул растворителя в газовую фазу.
Таким образом, над раствором давление насыщенного пара растворителя (Р) всегда меньше, чем над чистым растворителем (Р 0): Р < Р 0 . (Р 0 – Р)=∆P – понижение давления насыщенного пара растворителя над раствором. Отношение называется относительным понижением давления насыщенного пара растворителя.
В 1887 г. французский ученый химик Франсуа Рауль установил I закон: относительное понижение давления насыщенного пара растворителя над раствором равно мольной доле растворенного вещества.
Математическая запись I закона Рауля:
или ,
где N 2 – мольная доля растворенного вещества.
Выразив мольную долю растворенного вещества N 2 через соотношение , подставим данное равенство в выражениеI закона Рауля, выполнив необходимые преобразования, получим второй вариант записи I закона Рауля:
где N 1 – мольная доля растворителя.
Т.е. давление насыщенного пара над раствором равно его давлению над чистым растворителем, умноженному на мольную долю растворителя.
Кипение и замерзание растворов неэлектролитов. IIзакон Рауля.
Следствием понижения давления насыщенного пара растворителя над раствором будет:
понижение температуры замерзания раствора;
повышение температуры кипения раствора.
Рассмотрим диаграмму состояния воды и раствора неэлектролита. На рис.8.3 схематически изображена зависимость равновесного давления водяного пара от температуры над чистой водой и раствором.
При температуре кипения давление пара равно внешнему давлению, при температуре замерзания давление пара над веществом в жидком и твердом состояниях одинаково.
Линия АО – кривая сублимации – характеризует давление насыщенного водяного пара надо льдом, ОВ – кривая плавления или кристаллизации воды; ОС – кривая испарения или конденсации воды.
В точке О сосуществуют все три фазы воды: жидкость, пар, лед.
Линия О′С′ – кривая испарения или конденсации раствора;
О′В′ – кривая плавления или кристаллизации раствора.
Обозначение: t 1 - температура замерзания (кристаллизации) раствора при 760 мм рт. ст.; t 2 - температура замерзания чистой воды (0 °С при 760 мм рт. ст.); t 3 - температура кипения чистой воды (100 °С при 760 мм рт. ст.); t 4 - температура кипения раствора.
Поскольку
давление насыщенного пара воды над
раствором будет ниже, чем над чистой
водой, то изменение его давления будет
характеризоваться кривой О′С′, все
точки которой располагаются ниже
соответствующих точек кривой ОС для
чистого растворителя, т.е. кривая кипения
для раствора лежит ниже, чем для чистой
воды. Из рис. 8.3 видно, что при t
= 100 °С давление насыщенного пара воды
над раствором меньше атмосферного
давления (точка Е), поэтому при данной
температуре раствор не закипает.
Равенство давлений достигается в точке
D
при температуре t 4 .
При переходе от воды к раствору изменяется
также положение кривой плавления. И
кривая кипения, и кривая плавления
раствора расположены тем дальше от
соответствующих кривых воды, чем
концентрированнее раствор.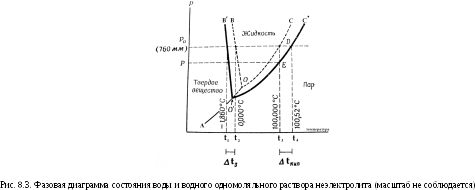
∆t кип = t 4 – t 3 = (t кип.р-ра – t кип.р-ля) – повышение температуры кипения раствора по сравнению с температурой кипения растворителя.
∆t зам = t 2 – t 1 = (t зам.р-ля – t зам.р-ра) – понижение температуры замерзания (кристаллизации) раствора по сравнению с температурой замерзания растворителя.
Зависимость ∆t кип и ∆t зам от концентрации растворов определяется вторым законом Рауля:
повышение температуры кипения и понижение температуры замерзания растворов пропорциональны моляльной концентрации растворенного вещества, т.е.
∆t кип = К эб · С m ,
∆t зам = К кр ·С m ,
где К эб – коэффициент пропорциональности, называемый эбуллиоскопической постоянной растворителя; К кр – криоскопическая постоянная растворителя; С m – моляльная концентрация растворенного вещества, моль/кг.
Физический смысл К эб и К кр : если С m = 1 моль/кг, то ∆t зам = К кр, т.е. К кр – понижение t зам раствора, моляльность которого равна 1 моль/кг; ∆t кип = К эб, т.е. К эб – повышение t кип раствора, моляльность которого равна 1 моль/кг.
К эб, К кр – характеристики растворителя, не раствора, зависят от природы растворителя (справочные величины). Например,
для воды: для бензола:
К кр =1,86 °С · кг/моль, К кр =5,12 °С · кг/моль,
К эб =0,52 °С · кг/моль; К эб =2,53 °С · кг/моль.
Для одномоляльных растворов различных неэлектролитов независимо от их состава температура кипения данного раствора повышается на одну и ту же величину, а температура замерзания – понижается на одну и ту же величину. Так, температура кипения различных по составу одномоляльных водных растворов увеличивается на 0,52°С, а температура замерзания понижается на 1,86°С.
Этот закон показывает, что свойства растворов зависят только от числа частиц растворенного вещества, но не от их размеров, природы и т.д.
Измерение понижения температуры кристаллизации раствора по сравнению с температурой кристаллизации чистого растворителя называют криоскопией. Измерение повышения температуры кипения раствора по сравнению с температурой кипения чистого растворителя называют эбуллиоскопией.
Методами криоскопии и эбуллиоскопии определяют относительные молекулярные массы растворенного неэлектролита. Для этого подставим в уравнение второго закона Рауля «развернутую» формулу для расчета моляльной концентрации растворенного вещества В
![]() =,
=,
∆t кип = К эб · ,
∆t зам = К кр · .
где М В - молярная масса растворенного неэлектролита В, численно равная его относительной молекулярной массе, m B – масса неэлектролита В, г; m р-ля – масса растворителя, кг.
Осмос. Осмотическое давление. Закон Вант-Гоффа.
Если привести в соприкосновение два раствора с разными концентрациями, то молекулы растворителя и растворенного вещества будут диффундировать в противоположных направлениях, преимущественно в том направлении, где их концентрация ниже. Такая двусторонняя диффузия приведет к выравниванию концентраций (С 1 = С 2).
Рассмотрим особый случай односторонней диффузии, когда на границе между раствором и растворителем или между двумя растворами различной концентрации находится перегородка, проницаемая для молекул растворителя и задерживающая частицы растворенного вещества.
Представим
себе, что в сосуд с водой опущен цилиндр
с раствором, нижняя часть которого
изготовлена из материала, пропускающего
растворитель, но не пропускающего
частицы растворенного вещества
(полупроницаемая перегородка). Получается
неравновесная система, т.к. если в воде
N 1 =1,
то в растворе мольная доля растворителя
– воды N 1 <1.
Поэтому в системе начнется самопроизвольный процесс выравнивания концентраций. Молекулы растворителя воды будут переходить в цилиндр с раствором (переход растворенного вещества исключен).
Односторонняя диффузия растворителя в раствор через полупроницаемую перегородку называется осмосом.
На рис. 8.4 представлен простейший прибор для наблюдения осмоса, называемый осмометром. В результате осмоса раствор поднимается по цилиндру вверх за счет того, что число молекул воды, проникающих в единицу времени в направлении от растворителя к раствору, больше числа молекул воды, проходящих через мембрану в обратном направлении. Через некоторое время подъем жидкости в цилиндре прекратится и ее уровень достигнет высоты h над уровнем жидкости в стакане. Столб жидкости с высотой h образовался за счет осмоса. Осмос прекращается тогда, когда скорости перехода молекул растворителя через полупроницаемую перегородку в обоих направлениях становятся одинаковыми.
Для количественной характеристики осмотических свойств растворов по отношению к чистому растворителю вводится понятие об осмотическом давлении. Осмотическое давление (Р осм ) – мера силы, приходящейся на единицу площади поверхности и заставляющей проникать молекулы растворителя через полупроницаемую перегородку или , другими словами, давление, которое нужно приложить к раствору, чтобы осмос прекратился. Осмотическое давление в растворе не существует, оно проявляется только тогда, когда раствор отделен от растворителя полупроницаемой мембраной.
Осмотическое давление Р осм зависит от температуры раствора и его концентрации и не зависит от природы растворителя и растворенного вещества. В 1886 г. голландский химик Вант-Гофф показал, что для разбавленных растворов неэлектролитов зависимость осмотического давления от температуры и концентрации выражается уравнением (закон Вант-Гоффа):
где Р осм – осмотическое давление раствора, кПа; С – молярная концентрация растворенного неэлектролита, моль/л; Т – абсолютная температура, К.
Заменим величину С отношением ;, где m – масса растворенного вещества, г; M – молярная масса растворенного вещества, г/моль; V – объем раствора, л. Подставим это отношение в выражение закона Вант-Гоффа:
Формально уравнение Вант-Гоффа аналогично уравнению состояния идеального газа и выражает сходство в поведении разбавленных растворов неэлектролитов с идеальными газами. Из вышеприведенного уравнения выразим величину М:
Данное выражение позволяет определить молекулярную массу растворенного вещества, измерив осмотическое давление в осмометре.
Явление осмоса играет важную роль в жизни растений, животных и человека. Стенки растительных клеток живых организмов представляют собой полупроницаемые мембраны, через которые свободно проходят молекулы воды, но почти полностью задерживаются вещества, растворенные в клеточном соке. Поэтому осмос служит причиной тургора (состояние напряжения) и плазмолиза (сморщивание) клеток. С ним связаны процессы усвоения пищи и обмена веществ. У высших животных и человека осмотическое давление в разных органах и тканях несколько меньше 8 атм и постоянно. Осмотическое давление широко встречается в природе, например, в скважинах осмотическое давление рвет породы и т.д.
Физическая химия: конспект лекций Березовчук А В
1. Общая характеристика растворов
Растворы – термодинамически устойчивые системы переменного состава, состоят не менее чем из двух компонентов и продуктов их взаимодействия. Это дисперсные системы, состоящие из дисперсной фазы и дисперсионной среды. Различают девять систем (табл. 1):
Таблица 1
Дисперсные системы
где Г – газ;
Т – твердое тело;
Ж – жидкость.
Существуют жидкие, газовые и твердые растворы . Растворы отличаются от химических соединений тем, что их состав может изменяться непрерывно. Как и любая химически равновесная в данных условиях система, растворы должны обладать минимумом свободной энергии Гиббса. По своему агрегатному состоянию дисперсные системы могут быть: газообразными, жидкими, твердыми; по степени дисперсности – взвесями, коллоидными и истинными растворами. Взвеси – гетерогенные системы, нестабильные во времени. Частицы их очень малы и сохраняют все свойства фазы. Взвеси расслаиваются, причем диспергированная фаза или выпадает в виде осадка, или всплывает в зависимости от соотношения плотностей. Примеры: туман (жидкость распределена в газе), суспензия (твердое тело – жидкость), эмульсия (жидкость – жидкость, C 2 H 5 OH + H 2 O – этиловый спирт и вода).
В истинном растворе распределенное в среде вещество диспергировано до атомного или молекулярного уровня. Примеры многочисленны: газообразный раствор – воздух, состоящий из главного компонента азота – 78% N 2 ; сплавы, представляющие собой твердые растворы, например, медные Cu – Zn, Cu – Cd, Cu – Ni и др.
Коллоидные растворы – микрогетерогенные системы, занимают промежуточное положение между истинными растворами и взвесями. Растворы состоят из растворенного вещества и растворителя. Растворителем считают тот компонент, который преобладает в растворе. Свойства растворов зависят от концентрации. Рассмотрим способы выражения концентрации растворов.
Из книги Революция в физике автора де Бройль Луи4. Общая теория относительности Остановимся теперь в нескольких словах на общей теории относительности. Вначале теория относительности была создана Эйнштейном лишь для инерционных систем координат, т е. для систем координат, движущихся прямолинейно и равномерно
Из книги Эволюция физики автора Эйнштейн АльбертОбщая теория относительности Остается выяснить еще один момент. Пока еще не решен один из наиболее фундаментальных вопросов: существует ли инерциальная система? Мы узнали кое-что о законах природы, их инвариантности по отношению к преобразованиям Лоренца и их
Из книги Эволюция физики автора Эйнштейн АльбертОбщая теория относительности и ее экспериментальная проверка Общая теория относительности пытается сформулировать физические законы для всех систем координат. Фундаментальная проблема теории относительности есть проблема тяготения. Теория относительности сделала
Из книги Гиперпространство автора Каку Мичио«Спойлер арифметики» и общая теория относительности В 1949 г. Эйнштейна обеспокоило открытие одного из его близких друзей и коллег, венского математика Курта Гёделя из Института перспективных исследований в Принстоне, где работал и Эйнштейн. Гёдель нашел внушающее
автора Березовчук А В2. Термодинамика растворов электролитов. Типы ДЭС На границе раздела фаз электрод – раствор происходит перераспределение зарядов, в результате которого у поверхности электрода накапливается избыток ионов какого-либо одного знака, в результате на поверхности возникает
Из книги Физическая химия: конспект лекций автора Березовчук А В3. Современные подходы к описанию термодинамических свойств растворов электролитов При теоретическом подходе к концентрированным растворам электролитов предпринимались попытки уточнить классическую модель теории Дебая – Хюккеля за счет учета следующих эффектов:1)
Из книги О чем рассказывает свет автора Суворов Сергей ГеоргиевичВторая характеристика света - его частота Длина волны - не единственная характеристика света. Другой его характеристикой является частота света. От длины волны света нетрудно перейти к его частоте. Для этого надо знать его скорость в пустоте, т. е. в пространстве, в
Из книги Гравитация [От хрустальных сфер до кротовых нор] автора Петров Александр НиколаевичГлава 6 Общая теория относительности Каждый из магов имеет свой предел… [они] могут, скажем, останавливать время, но только в римановом пространстве и ненадолго. Аркадий Стругацкий, Борис Стругацкий «Понедельник начинается в субботу» Предпосылки построения ОТО Наконец,
Из книги Теория относительности для миллионов автора Гарднер Мартин5. Общая теория относительности В начале гл. 2 мы указывали, что есть два пути обнаружить абсолютное движение: измерять движение по отношению к пучку света и использовать явление инерции, возникающее при ускорении предмета. Опыт Майкельсона - Морли показал, что первый
Из книги Движение. Теплота автора Китайгородский Александр ИсааковичКипение растворов Явление кипения растворов имеет много общего с явлением замерзания.Наличие растворенного вещества затрудняет кристаллизацию. По тем же самым причинам растворенное вещество затрудняет и кипение. В обоих случаях чужие молекулы как бы борются за
Из книги Астероидно-кометная опасность: вчера, сегодня, завтра автора Шустов Борис Михайлович10.9. Сравнительная характеристика способов противодействия В этом разделе рассмотрены различные способы противодействия угрожающему телу. Перечислим основные способы воздействия на космические объекты, угрожающие столкновением с Землей, которые предлагались в
Из книги Новый ум короля [О компьютерах, мышлении и законах физики] автора Пенроуз РоджерРастворы имеют большое значение в жизни и практической деятельности человека. Так, процессы усвоения пищи человеком и животными связаны с переводом питательных веществ в раствор. Растворами являются все важнейшие физиологические жидкости (кровь, лимфа и т.д.). Производства, в основе которых лежат химические процессы, обычно связаны с использованием растворов.
Растворы – многокомпонентные гомогенные системы, в которых одно или несколько веществ распределены в виде молекул, атомов или ионов в среде другого вещества – растворителя.
Раствор может иметь любое агрегатное состояние – твердое, жидкое или газообразное. Всякий раствор состоит из растворенных веществ и растворителя. Обычно растворителем считают тот компонент, который в чистом виде существует в таком же агрегатном состоянии, что и полученный раствор (например, раствор соли в воде: соль – растворенное вещество, вода – растворитель). Если оба компонента до растворения находились в одинаковом агрегатном состоянии (например, спирт и вода), то растворителем считается компонент, находящийся в большем количестве.
По структуре растворы занимают промежуточное положение между механическими смесями и химическими соединениями. С механическими смесями их роднит переменность состава, а с химическими соединениями – однородность состава по всей фазе и наличие теплового эффекта при образовании. В соответствии с этим первое время существовали две противоборствующие теории: "физическая" и "химическая", каждая из которых отстаивала свои взгляды на строение растворов.
Современные представления о строении растворов основываются на сольватной теории, выдвинутой Менделеевым и развитой его последователями. Согласно этой теории, в системе при растворении одновременно происходит два процесса: диффузия растворяемого вещества в объеме растворителя (физический процесс) и образования из молекул растворителя и растворяемого вещества нестойких соединений переменного состава – сольватов (химический процесс). Если растворителем служит вода, то эти соединения называют гидратами.
Образование растворов является процессом самопроизвольным, идущим с увеличением беспорядка системы, т.е. с повышением энтропии. Например, при растворении кристалла система из полностью упорядоченного состояния переходит в менее упорядоченное. При этом с увеличением энтропии (AS > 0) уменьшается свободная энергия системы (AG <0).
Если раствор образуется из 2 жидкостей, то движущая сила процесса растворения обусловлена стремлением компонентов раствора к выравниванию концентраций, что также приводит к увеличению энтропии, т.е. AS > 0, a AQ < 0. Растворение вещества – процесс обратимый. И как всякий обратный процесс, растворение заканчивается установлением динамического равновесия: нерастворенное вещество – вещество в растворе. Раствор, находящийся в равновесии с растворяющимся веществом, называют насыщенным раствором, а достигнутую предельную концентрацию насыщенного раствора – растворимостью.
Важнейшей характеристикой раствора является его состав или концентрация компонентов.
Концентрация растворов – количество растворенного вещества, содержащееся в определенном количестве раствора или растворителя.
Концентрацию растворов можно выражать по-разному. В химической практике наиболее употребительны следующие способы выражения концентраций:
1. Массовая доля растворенного вещества (процентная концентрация) – показывает, сколько граммов вещества растворено в 100 г раствора. Она определяется по формуле:
где W – массовая доля растворенного вещества,
m в-ва – масса растворенного вещества,
m р-ра – масса раствора.
2. Молярная концентрация – показывает, сколько молей растворенного вещества содержится в 1 л раствора.
3. Моляльная концентрация – показывает, сколько молей вещества содержится в 1 кг растворителя.
Растворы газов в жидкостях
Растворимость газов в жидкостях зависит от их природы, природы растворителя, температуры и давления. Как правило, растворимость газа больше, если растворение сопровождается химическим взаимодействием его с растворителем, и меньше, если при этом химического взаимодействия не происходит. Например, в 1 л воды при н.у. растворяется 0,0002 г водорода, не взаимодействующего с водой, и 875 г аммиака, который реагирует с водой с образованием гидроксида аммония.
Зависимость растворимости газов от природы растворителя можно показать на следующих примерах. При одинаковых условиях в 1000 г воды растворяется 87,5 г NH 3 , а в 100 г этилового спирта – только 25 г. Растворимость газов в значительной мере зависит от температуры. При повышении температуры растворимость их уменьшается, а при понижении увеличивается. Так при 0 0 С в 100 мл воды растворяется 171 см 3 СО 2 , при 20 0 С – только 87,8 см 3 . Поэтому длительным кипячением можно почти полностью удалить растворенные газы из жидкости, а насыщение жидкостей газом целесообразно проводить при низких температурах.
Растворимость газа зависит также от давления. Зависимость растворимости газа от давления определяется законом Генри .
С = к · р, (4.2)
где С – концентрация газа в растворе,
к – коэффициент пропорциональности, зависящий от природы жидкости и газа,
р – давление газа над раствором.
Масса растворенного газа при постоянной температуре прямо пропорциональна давлению газа над раствором.
Закон Генри справедлив только для разбавленных растворов в условиях низких давлений. Газы, вступающие во взаимодействие с растворителем NH 3 , SO 2 , HC1 с водой, закону Генри не подчиняются. Их растворимость также увеличивается с повышением давления, но по более сложному закону.
Проявление закона Генри иллюстрируется образованием обильной пены при откупоривании бутылки с газированной водой или бутылки с шампанским; здесь происходит резкое уменьшение растворимости газа при понижении его парциального давления. Этот же закон объясняет возникновение кессонной болезни. На глубине 40 м ниже уровня моря общее давление составляет 600 кПа и растворимость азота в плазме крови в 9 раз больше, чем на поверхности моря. При быстром подъеме водолаза с глубины растворенный азот выделяется в кровь пузырьками, которые закупоривают кровеносные сосуды, что может привести к тяжелым последствиям.
Растворимость газа уменьшается при наличии в растворе третьего компонента. Так, в растворах электролитов газы растворяются значительно хуже, чем в чистой воде. Например, в 1 г воды при 0 0 С растворяется 3 · 10 3 м 3 хлора, а в 1 г насыщенного раствора NaCl растворяется в 10 раз меньше, поэтому при хранении хлора над жидкостью воду заменяют на раствор хлорида натрия.
Леккия №17
РАСТВОРЫ
Общая характеристика растворов.
Способы выражения концентрации растворов.
Термодинамика и механизм процесса растворения.
Растворимость.
Вода как растворитель. Значение растворов в жизнедеятельности организмов
1. Общая характеристика растворов.
Растворы – это гомогенные системы переменного состава, включающие два и более компонентов. Частицы компонентов раствора распределены по его объему в виде атомов, молекул или ионов (размер частиц 0,1 – 0,5 нм).
Образование растворов, в отличие от механических смесей, сопровождается изменением энтальпии, энтропии и объема системы.
По агрегатному состоянию различают газовые, жидкие и твердые растворы. Но обычно термин растворы относится к жидким системам.
2. Способы выражения концентрации растворов.
Относительное содержание компонентов в растворе определяется его концентрацией.
Молярная концентрация – это количество вещества, содержащееся в одном литре раствора (моль/л):
Э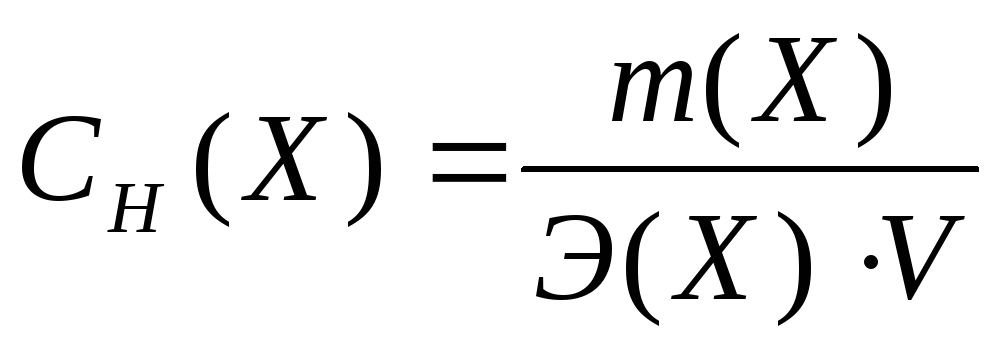 квивалентная
концентрация
– это число молей
эквивалентов вещества, содержащихся в
одном литре раствора (моль/л):
квивалентная
концентрация
– это число молей
эквивалентов вещества, содержащихся в
одном литре раствора (моль/л):
Эквивалент – это реальная или условная частица вещества, которая в кислотно-основной реакции эквивалентна одному иону водорода, а в окислительно-восстановительной эквивалентна одному электрону.
Масса одного моля эквивалентов называется молярной массой эквивалента вещества (Э). В разных реакциях одно и то же вещество может иметь разные эквиваленты.
Моляльная концентрация – это количество вещества, содержащееся в одном килограмме растворителя (моль/кг):
М ассовая
доля
равна отношению массы растворенного
вещества к массе раствора:
ассовая
доля
равна отношению массы растворенного
вещества к массе раствора:
М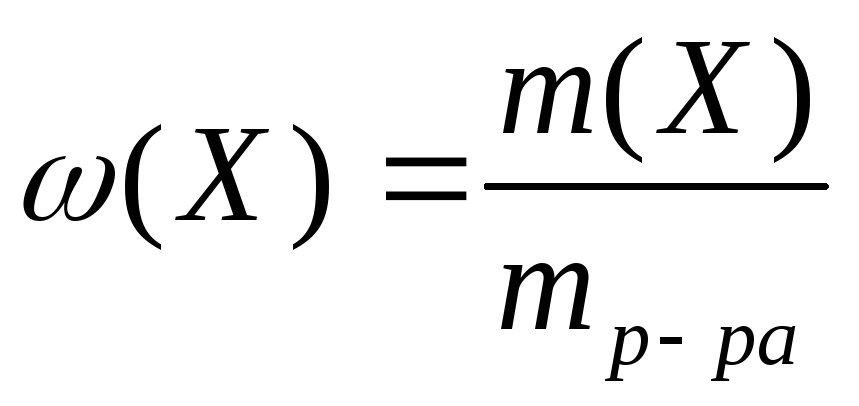 олярная
доля
равна отношению количества
растворенного вещества в общему
количеству веществ в растворе:
олярная
доля
равна отношению количества
растворенного вещества в общему
количеству веществ в растворе:
К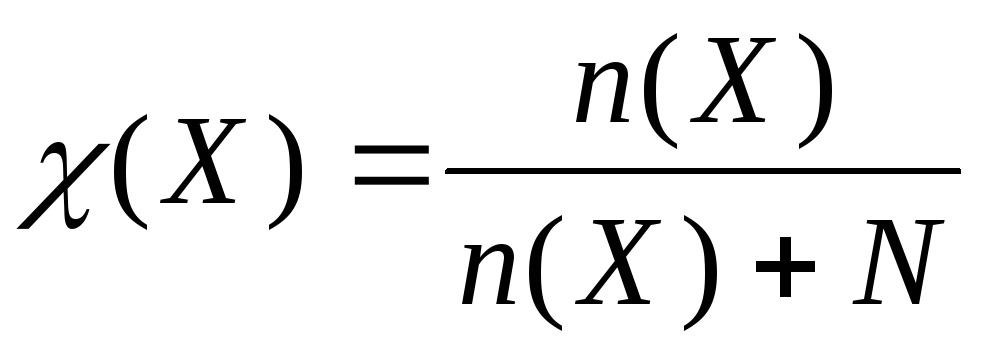 ак
правило, вещество обладает определенной
растворимостью в данном растворителе.
Подрастворимостью
понимают
концентрацию вещества в насыщенном
растворе.
ак
правило, вещество обладает определенной
растворимостью в данном растворителе.
Подрастворимостью
понимают
концентрацию вещества в насыщенном
растворе.
3. Термодинамика и механизм процесса растворения
Растворение – сложный физико-химический процесс, включающий три основные стадии, каждая из которых характеризуется изменениями термодинамических функций Н иS:
разрушение химических и межмолекулярных связей в растворяемом веществе (например, разрушение кристаллической решетки): Н 1 >0,S 1 >0
химическое взаимодействие частиц растворенного вещества с растворителем (сольватация): Н 2 <0,S 2 <0
равномерное распределение частиц растворенного вещества в среде растворителя путем диффузии: Н 3 >0,S 3 >0
Согласно 2-му закону термодинамики условием самопроизвольности процесса растворения является убыль энергии Гиббса:
G=H-TS< 0,
которая складывается из энтальпийного Н и энтропийногоTSфакторов.
Растворение газов в жидкостях приводит к упорядочению системы и, следовательно, сопровождается уменьшением энтропии: S р-ния <0. Движущей силой процесса растворения в этом случае является энтальпийный фактор и растворение большинства газов является процессом экзотермическим:Н р-ния <0. Таким образом, самопроизвольное растворение газов возможно при низких температурах (|Н| > |TS|)
Растворение жидких и твердых веществ в жидкостях приводит к увеличению беспорядка в системе и увеличению энтропии: S р-ния >0. Суммарный тепловой эффект процесса растворения определяется в основном слагаемымиН 1 иН 2 и в зависимости от их соотношения может и быть и положительным (NaCl), и отрицательным (NaOH). Растворение большинства кристаллических веществ – процесс эндотермическийН р-ния >0, так как энергия, затрачиваемая на разрушение кристаллической решетки не компенсируется энергией, выделяемой за счет сольватации. Таким образом, самопроизвольному растворению большинства твердых веществ способствуют высокие тепмературы (|Н| < |TS|).
Растворы, образование которых не сопровождается изменениями объема системы и тепловыми эффектами (V=0,Н=0), называютидеальными . Движущей силой образования идеального раствора является увеличение энтропии системы. Идеальный раствор – понятие абстрактное. Реальные системы могут лишь приближаться к идеальным. Наиболее близки к модели идеального раствора системы, в которых компоненты близки по свойствам и практически не взаимодействуют друг с другом (например, раствор толуола в бензоле). Приближаются по свойствам к идеальным бесконечно разбавленные растворы, в которых взаимодействиях сводятся к минимуму за счет низкой концентрации растворенного вещества.
4. Растворимость
Под растворимостью понимают концентрацию растворенного вещества в насыщенном растворе.
Растворимость выражают в тех же единицах, что и концентрацию. Часто используют коэффициент растворимости s, равный массе растворенного вещества (г) в насыщенном растворе, содержащем 100 г растворителя.
Насыщенным называют раствор, который находится в равновесии с избытком растворяемого вещества (G р-ния =0). Насыщенный раствор имеет максимально возможную в данных условиях концентрацию.
Растворимость зависит:
от природы растворенного вещества и растворителя;
от температуры;
от давления;
от присутствия третьих компонентов.
Влияние природы компонентов на растворимость определяется принципом:подобное растворяется в подобном . Полярные растворители, например, вода, хорошо растворяют вещества с ионной связью (неорганические соли, кислоты и основания). Хорошей растворимостью в воде обладают полярные органические соединения, образующие с молекулами растворителя водородные связи (спирты, карбоновые кислоты, амины). Неполярные растворители, например, углеводороды, растворяют неполярные и малополярные соединения (жиры).
Влияние температуры на растворимость зависит от теплового эффекта растворения и определяется принципом Ле Шателье. Повышению растворимости газов способствует понижение температуры, так как растворение газов – процесс экзотермический. Растворимость большинства твердых веществ и жидкостей - процесс эндотермический и возрастает при повышении температуры.
Влияние давления существенно только в том случае, если при растворении происходит значительное изменение объема системы, что наблюдается при растворении газов в жидкостях. Растворимость газов растет с увеличением давления, так как сопровождается уменьшением объема системы.
Закон Генри:
Количество газа, растворенного в определенном объеме жидкости при постоянной температуре прямо пропорционально давлению газа.
c (X ) = K г p (X )
где c(X) – молярная концентрация газа,моль/л
K г - константа Генри, моль/лПа
p(X) – давление газа над раствором, Па
Влияние присутствия третьих компонентов.
Растворимость газов в жидкостях значительно снижается в присутствии электролитов (солей) Этот процесс называют высаливанием .
Закон Сеченова:
Растворимость газов в жидкостях в присутствии электролитов понижается.
С(X) = С 0 (X)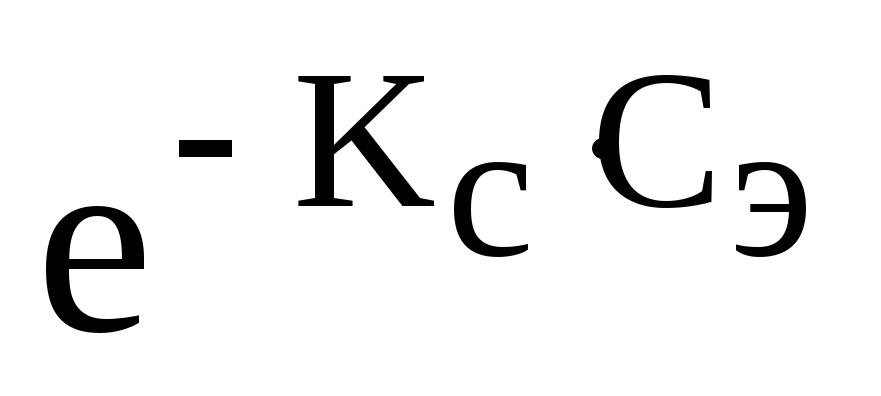
где С(X) – растворимость газа в присутствии электролита
С 0 (X) – растворимость газа в чистом растворителе
К С - константа Сеченова
С э - концентрация электролита
Биологическое значение законов Генри и Сеченова.
Изменение растворимости газов в крови при изменении давления может привести к тяжелым заболеванием. Кесонная болезнь у водолазов – проявление закона Генри. В соответствии с законом Сеченова растворимость кислорода и углекислого газа в крови зависит от концентрации электролитов, а также белков, липидов и других веществ.
5. Вода как растворитель. Значение растворов в жизнедеятельности организмов
Самым распространенным растворителем на нашей планете является вода. У животных и растительных организмов содержание воды составляет обычно более 50%, а в ряде случаев достигает 90-95%.
Вода хорошо растворяет многие ионные и полярные соединения. Такое свойство воды связано с ее высокой диэлектрической проницаемостью (= 78,5). В результате многие ионные соединения диссоциируют и отличаются высокой растворимостью в воде. Другой класс веществ, хорошо растворимых в воде, составляют полярные органические соединения (спирты, альдегиды, кетоны). Их растворимость обусловлена образованием водородных связей с молекулами воды.
Важны и другие аномальные свойства воды: высокое поверхностное натяжение, низкая вязкость, высокие температуры плавления и кипения, более высокая плотность в жидком состоянии, чем в твердом.
Вследствие высокой полярности вода вызывает гидролиз веществ (эфиров, амидов и др.). Так как вода составляет основную часть внутренней среды организма, то она обеспечивает процессы всасывания, передвижения питательных веществ и продуктов обмена в организме.
Важнейшие биологические жидкости – кровь, лимфа, моча, слюна, пот являются растворами солей, белков, углеводов, липидов в воде. Биохимические процессы в живых организмах протекает в водных растворах.
В жидких средах организма поддерживается постоянство рН, концентрации солей и органических веществ, постоянство осмотического давления. Такое постоянство называется гомеостазом. Приведенные примеры показывают, что учение о растворах представляет особый интерес для медиков.




